Alkuainetaulukon 150-vuotisjuhlavuosi vuonna 2019
Dmitri Mendelejevin alkuainetaulukko
Vuosi 2019 on alkuaineiden jaksollisen järjestelmän kansainvälinen 150-vuotisjuhlavuosi. Alkuaineiden jaksollista järjestelmää, eli alkuainetaulukkoa juhlitaan nyt, koska vuonna 1869 Dmitri Mendelejev julkaisi ensimmäisen version alkuainetaulukostaan. Mendelejev työskenteli tuolloin Pietarin yliopistossa ja hän esitteli alkuainetaulukkonsa ensin venäläiselle tiedeyhteisölle. Hänellä oli kuitenkin myös tiiviit yhteydet Keski-Euroopan tiedeyhteisöön ja alkuainetaulukko julkaistiin vielä samana vuonna myös saksankielisessä Zeitschrift für Chemie -julkaisusarjassa.
Alkuainetaulukon rakennuspalikat
Mendelejev ei luonnollisestikaan johtanut alkuainetaulukkoaan tyhjästä, vaan rakensi sen parhaan olemassa olevan tieteellisen tiedon pohjalta. Enemmistö luonnossa esiintyvistä alkuaineista tunnettiin jo vuonna 1869 ja useat kemistit olivat 1800-luvun aikana kehitelleet teorioita alkuaineiden luokittelemiseksi. John Dalton hahmotteli 1800-luvun alussa atomiteorian, joka oli merkittävä askel atomipainojen systemaattiselle mittaamiselle. Vuoteen 1869 mennessä tunnettujen alkuaineiden atomipainot oli pystytty määrittämään kohtuullisella tarkkuudella, mikä oli tärkeä edellytys alkuainetaulukon rakentamiselle.
Atomipainojen lisäksi alkuaineiden lajittelua oli tehty myös niiden kemiallisten ominaisuuksien perusteella. Johann Wolfgang Döbereiner oli havainnut jo 1820-luvun lopussa, että tiettyjä alkuaineita oli mahdollista lajitella ominaisuuksiensa perusteella kolmen ryhmiin, triadeihin. Triadeja olivat esimerkiksi Li-Na-K, Ca-Sr-Ba ja Cl-Br-I. Döbereiner myös havaitsi, että triadin keskimmäisen alkuaineen atomipaino vastasi suunnilleen triadin kevyimmän ja raskaimman alkuaineen atomipainon keskiarvoa.
Ratkaisevat ennusteet
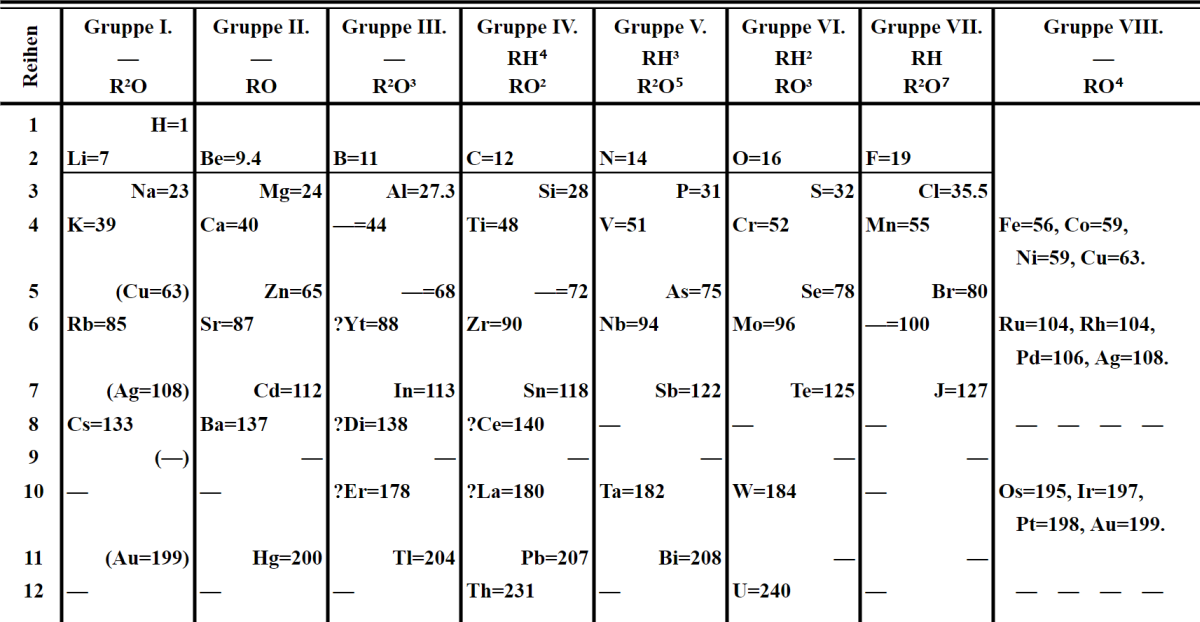
Mendelejev oli liikkeellä oikeaan aikaan, sillä samoihin aikoihin 1860-luvun loppupuolella omia alkuainetaulukoitaan työstivät mm. Julius Lothar Meyer Saksassa ja John Newlands Englannissa. Miksi juuri Mendelejevin vuonna 1869 julkaisemaa taulukkoa (Kuva 1) sitten juhlitaan ja häntä pidetään alkuainetaulukon kehittäjänä? Merkittävin syy tähän lienee se, että taulukkoaan kehittäessään Mendelejev teki aivan uusia havaintoja alkuaineiden jaksollisuudesta ja näin hänestä tuli ensimmäinen kemisti, joka hyödynsi alkuainetaulukon ennustusvoimaa.

Laittaessaan alkuaineita järjestykseen atomipainojen ja kemiallisten ominaisuuksien avulla Mendelejev huomasi, että taulukossa on selviä aukkopaikkoja, joista puuttuu alkuaine. Näin hän ennusti esimerkiksi germaniumin olemassaolon 17 vuotta ennen kuin se eristettiin luonnosta. Mendelejev kutsui germaniumia ”eka-piiksi” ja julkaistessaan alkuainetaulukkonsa toisen version vuonna 1871 (Kuva 2) hän ennusti hyvin tarkasti germaniumin atomipainon ja tiheyden. Koska Mendelejevin ennustukset olivat hyvin perusteltuja ja selkeästi todennettavissa, ne myös innostivat muita tutkijoita uusien alkuaineiden etsintään. Kun Mendelejevin ennustamia alkuaineita sitten löydettiin ja niiden ominaisuuksien havaittiin vastaavan ennustettuja, oli se paras mahdollinen tunnustus Mendelejevin työlle.
Alkeishiukkaset alkuainetaulukon taustalla
Mendelejevin ja muiden 1800-luvun kemistien saavutukset alkuaineiden lajittelemiseksi ovat hämmästyttäviä, kun ottaa huomioon, että heillä ei ollut mitään tietoa alkeishiukkasista, jotka oikeasti määräävän alkuainetaulukon rakenteen. Alkuaineiden järjestys taulukossa määräytyy alkuaineiden järjestysluvun Z, eli atomiytimen protonien lukumäärän mukaan. Atomipainot toki kasvavat suunnilleen samaan tahtiin kuin järjestysluku, mutta joidenkin alkuaineiden atomipaino onkin pienempi kuin edellisen alkuaineen atomipaino (esimerkiksi nikkelin, Z = 28, atomipaino on pienempi kuin koboltin, Z = 27).
Atomipainojen epäjärjestelmällinen käyttäytyminen ja epätarkkuudet atomipainojen määrityksessä aiheuttivat sekaannuksia alkuainetaulukon lopullisen rakenteen osalta, kunnes Henri Moseley osoitti 1913 röntgenspektroskopian avulla, että alkuaineiden järjestyksen määrääkin järjestysluku Z eikä atomipaino. Moseleyn tutkimukset perustuivat jo tukevasti 1900-luvun alussa kehitettyyn kvantti- ja atomiteoriaan ja saman kvanttimekaanisen mullistuksen tuloksena mukaan kuvaan saatiin myös kemian keskeisimmät pelurit, eli elektronit.
Kemia on valenssielektronien tiede. Kvanttimekaniikan huima kehitys 1900-luvun alkuvuosikymmeninä toi kemistien käyttöön lukuisia teoreettisia käsitteitä ja mittausmenetelmiä, joilla alkuaineiden kemialliset sidokset ja erot eri alkuaineiden kemiallisessa reaktiivisuudessa pystyttiin selittämään. Röntgenkristallografia mahdollisti ensi kertaa kemiallisten yhdisteiden atomitason rakenteiden tarkastelun ja alkuainetaulukon kemialliset trendit pystyttiin ymmärtämään alkuaineiden valenssielektronirakenteen pohjalta. Esimerkiksi alkalimetallien ja halogeenien muodostamat suolat voidaan ymmärtää yhdisteinä, joissa alkalimetalliatomi luovuttaa ainoan valenssielektroninsa halogeeniatomille, joka kaipaa kovasti yhtä lisäelektronia.
Alkuainetaulukoita joka lähtöön
Alkuaineen järjestysluku Z on täysin yksikäsitteinen tapa järjestää alkuaineet jonoon. Alkuainetaulukon toinen tärkeä ulottuvuus on kuitenkin alkuaineen kemiallinen luonne, eli valenssielektronirakenne. Koska alkuaineen kemiallista luonnetta voi tarkastella niin monesta eri näkökulmasta, alkuainetaulukon voisi periaatteessa järjestää lukuisilla eri tavoilla. Mark Leach on koonnut mielenkiintoisen tietokannan The Internet Database of Periodic Tables, joka sisältää satoja erilaisia alkuainetaulukoita 1800-luvulta alkaen.
Nykyaikaisen, tunnistettavan muotonsa alkuainetaulukko sai 1940-luvulla, kun Glenn T. Seaborg järjesti aktinoidit samalla tavalla kuin lantanoidit. Seaborg löysi kollegoineen useita uraania raskaampia alkuaineita ja hän havaitsi, että aktinoidit on syytä käsitellä erillisenä kokonaisuutena. Seaborgin vuonna 1945 julkaisema alkuainetaulukko on jo hyvin lähellä nykyisin käytettyä IUPACin jaksollista järjestelmää.
Alkuainetaulukoiden tietokanta sisältää myös lukuisia uudelleentulkintoja viime vuosikymmeniltä aina vuoteen 2019 asti. Mistä alkuainetaulukon uudelleentulkinnoissa sitten on kyse, eivätkö kaikki olekaan tyytyväisiä nykytilaan? Eivät ole, sillä tyypillisiä kiistakapuloita ovat mm. heliumin paikka, jalokaasujen sijoittuminen ylipäänsä ja ryhmän 3 koostumus (miten lantanoidit ja aktinoidit mainitaan). Osan uudelleentulkinnoista voi kuitata huumorilla ja osassa graafisesti näyttävä esitystapa on ollut tieteellisiä perusteita merkittävämmässä roolissa. Mutta osa uudelleentulkinnoista on tehty tositarkoituksella ja näistä sitten väännetään tiukkaankin sävyyn esimerkiksi kemian filosofiaan suuntautuneissa julkaisusarjoissa. Toistaiseksi näistä väännöistä ei ole ollut tuloksena merkittäviä mullistuksia alkuainetaulukon rakenteeseen.
Alkuainetaulukko on kemistin tiekartta
Alkuainetaulukko on siis 150-vuotta vanha käsite, joka hioutui nykyaikaiseen muotonsa jo yli 70 vuotta sitten. Miksi alkuainetaulukko on edelleen kemiassa niin keskeisessä roolissa?
Minusta alkuainetaulukon menestyksen salaisuus on siinä, että se näyttää yksinkertaiselta, mutta sitä voi soveltaa salamannopeasti hyvinkin monimutkaisiin kemian ongelmiin. Alkuainetaulukko on kemistin tiekartta, joka tarjoaa meille oikotien valenssielektronien sielunelämään. Sen avulla voimme mm. selittää olemassa olevien yhdisteiden rakenteet ja ominaisuudet, mutta alkuainetaulukon mahtavin ominaisuus on kuitenkin sen ennustava voima, jonka Mendelejev valjasti käyttöönsä 150 vuotta sitten. Alkuainetaulukon silmäily vaikkapa kahvitauon aikana voi synnyttää ratkaisevan tärkeän ajatuksen siitä, miten yhdisteen alkuainekoostumusta kannattaisi alkaa säätää, jotta sen rakenne ja ominaisuudet muuttuisivat haluttuun suuntaan.
Alkuainetaulukko on ollut kemistien luovuuden lähde 150 vuoden ajan ja toivotan sille pitkää ikää uusien jännittävien yhdisteiden ja materiaalien alkulähteenä!